弹性体的玻璃化转变温度(Tg)低于室温,且具有可逆变形能力。弹性性能对于维持天然生物组织(如心脏、肺、血管、皮肤等)及人造结构(如密封垫圈、软管、轮胎等)的功能至关重要。共价键将无规卷曲的聚合物连接形成弹性体,如弹性蛋白、硫化橡胶等,其化学性质决定了在弹性体中的交联网络结构。而弱键交联弹性体通常表现为更大的塑性。因此,一般需对聚合物进行设计来获得特定功能的弹性体,这使得弹性体的制备变得困难,并限制了其通用性和应用范围。如何设计合适的键合作用来获得特定功能的弹性体呢?这变得非常重要。
【工作亮点】
针对这一问题,近期美国康奈尔大学王亚冬教授团队开展了系统深入的研究,考察了配位键类型、配体类型、聚合物主链和金属离子种类,通过将高度通用的、弱于共价键但强于弱键键合作用的螯合键引入到弹性体中,通过调控不同种类金属离子与配体螯合,开发了不同机械性能和生物降解性的弹性体。与广泛使用的生物材料聚己内酯相比,小鼠模型显示其与皮下组织的相容性更高,降解后植入部位恢复正常,所报道的生物可降解弹性体将为生物医学以及其他领域提供更多可能性。相关工作以“Chelation Crosslinking of Biodegradable Elastomers”为题发表在国际材料学领域顶级期刊《先进材料》(Advanced Materials)。
【图文分析】
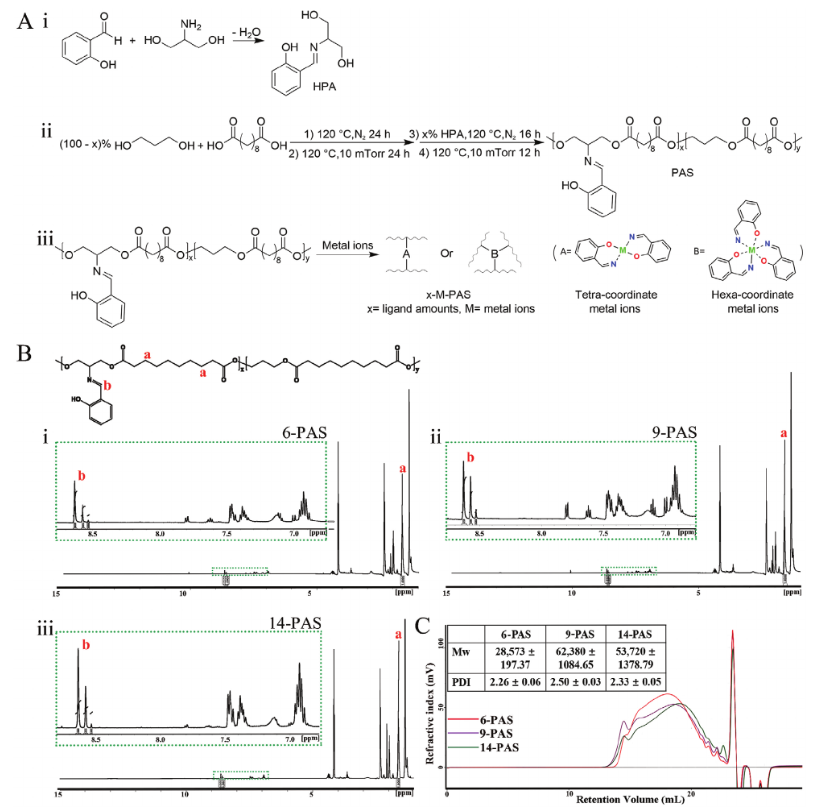
带有两个羟基和一个酚的席夫碱配体HPA是通过简单的缩合反应合成的,癸二酸、1,3-丙二醇和HPA缩聚反应产生聚丙二醇-co-(羟基苯基亚甲基)氨基丙二醇癸二酸酯)(PAS)嵌段共聚物,1,3-丙二醇和HPA的羟基转化为聚酯骨架的酯键,而酚氧基和席夫碱则作为侧基,通过调节二醇中HPA的摩尔百分比,可以合成出含有三种不同密度的配体体(分别为6%,9%和14%)的PAS聚合物。该嵌段聚合物可结合多种金属离子发生螯合作用,且一个配体可结合多个金属离子以产生不同强度的键合作用,从而制备具有不同特性的弹性体。添加金属离子(例如铁)后PAS溶液立即凝胶化,表明发生交联;在竞争性配体存在下,螯合键应该是可逆的,在加入乙二胺四乙酸(EDTA)的1分钟内,凝胶又变成溶液。
图1 材嵌段聚合物设计和表征
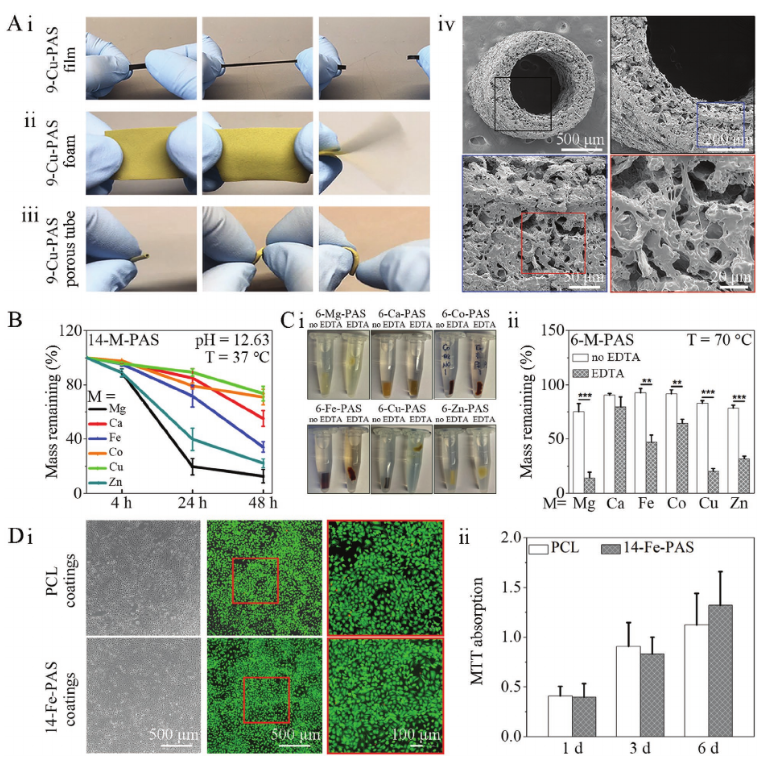
未交联的PAS聚合物可以加工成各种形状,因为它会熔化成液体并溶于常见的有机溶剂,例如丙酮、四氢呋喃等;将M-PAS制成薄膜、泡沫和多孔管,以9-Cu-PAS为例,薄膜和泡沫表现出优异的弹性,9-Cu-PAS多孔管的孔隙率约为65%,可以反复扭曲而不会变形。M-PAS的酯骨架通过水解降解,在含有NaOH的PBS溶液中可加速体外降解,M-PAS弹性体的降解速率随金属离子而变化,与它们不同的金属-配体螯合强度有关。弹性体形成过程中金属-配体发生交联,其螯合键的不同强度决定了交联聚合物的稳定性,在EDTA存在下,6-M-PAS更快降解表明金属配位键将聚合物网络保持在一起,并且交联可以被另一个配体逆转,这提供了控制聚合物降解的一种新方法。MTT分析证明对14-Fe-PAS和PCL具有相同的代谢活性,结果表明,14-Fe-PAS至少在体外具有与PCL相同的细胞相容性。
图2 M-PAS的多功能性、降解性和细胞相容性
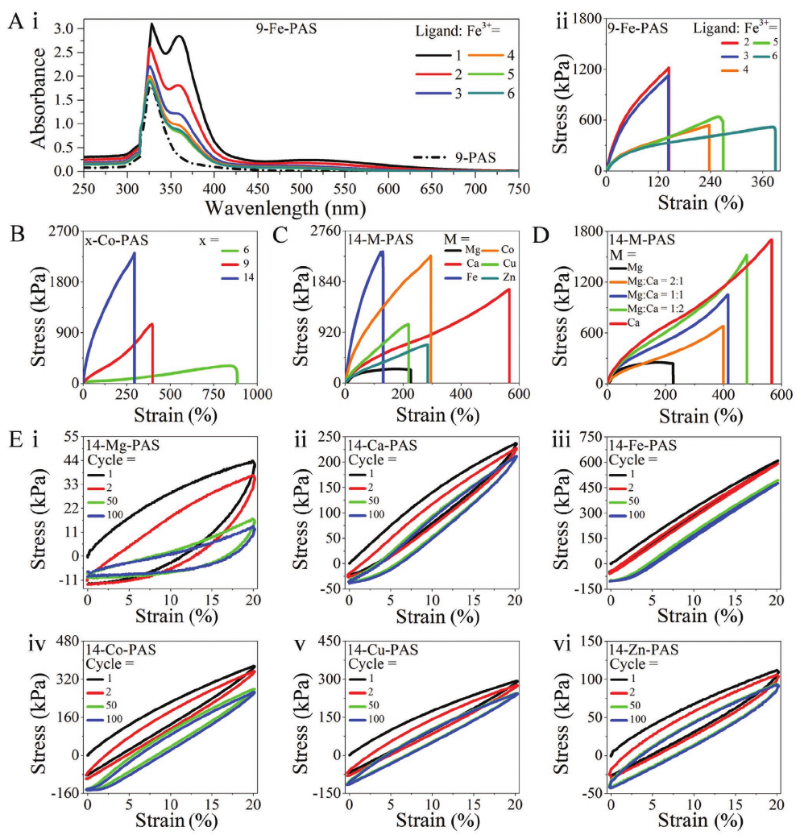
以9-Fe-PAS为例,研究发现通过控制交联可获得不同机械性能的弹性体,当配体/金属的摩尔比从2增加到6时,断裂应变从144± 9.20%增加至394 ± 42.6%,拉伸强度从1127 ± 57.86降低至552 ± 55.59 kPa,杨氏模量从2125± 190.25减少至674 ±121.34 kPa,韧性保持在1000 kJ m – 3左右。Fe3+含量减少,薄膜更柔韧具有更高的可拉伸性,较少的交联剂导致交联之间的聚合物链更长,从而更具弹性。在给定的配体密度下,不同的金属具有不同的螯合键强度,对于选择金属离子获得具有特定机械性能的弹性体以满足特定应用的需求至关重要。通过配位键交联的优点是可以在同一聚合物网络中使用金属离子的混合物。对14-M-PAS膜进行了磁滞测试,所有薄膜都可以承受至少100个循环的循环载荷而不会破裂,金属离子决定了14-M-PAS的弹性反冲力,随着循环的增加,应力降低表明键断裂会耗散能量,Fe3+交联聚合物弹性最大,表明Fe3+与PAS的强烈螯合,弹性主要来源于金属离子螯合键的快速动态缔合和解离。
图3 通过配体/金属比、配体密度和金属离子类型调控M-PAS机械性能
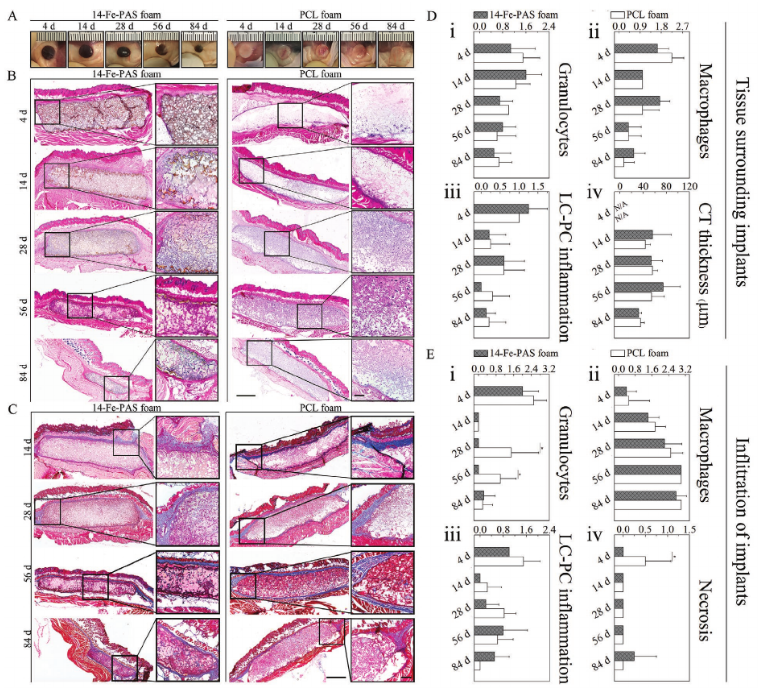
以14-Fe-PAS为例,通过小鼠皮下植入评估生物相容性。以生物相容性良好的PCL作为对照,将大小相同的14-Fe-PAS泡沫和PCL泡沫对称地植入同一只小鼠的背部,所有小鼠均存活下来,在植入部位无感染;14天后,植入物边缘可见明显的圆滑,这可能是由于降解所致,第28天细胞渗透到整个具有纤维血管组织的植入物中并且开始大量降解,这是由聚合物含量降低所致,组织学分析表明大多数14-Fe-PAS在第84天时已降解,而在84 d后PCL植入物仍保持其形状,尺寸变化不大。以上结果表明14-Fe-PAS在体内的降解速度比PCL快,且其降解速率比体外的PCL高4.67倍。然而,14-Fe-PAS和PCL植入物周围的组织均显示出轻微的不良反应,如炎症和纤维化,但PCL的炎症反应比14-Fe-PAS稍强,14-Fe-PAS的降解速度比PCL快,在植入部位的微环境中降解产物的浓度更高,在皮下环境中,14-Fe-PAS诱导的炎症反应比PCL轻。
图4 在小鼠皮下植入14-Fe-PAS泡沫及其可降解性
【总结】
本文研究了金属交联螯合键在生物降解弹性体中的多功能性,通过在聚合物中引入不同类型的金属离子,调控金属与配体的比例以及聚合物中的配体密度,可获得系列可调机械性能的弹性体,其生物相容性与PCL生物相容性相匹配,为可生物降解弹性体的发展开辟了新的途径,以改善软组织的重建和再生。本文提出的金属离子螯合交联机理为许多新的研究提供了可能,如引入不同类型的金属离子、探索其他类型的配体等,为赋予弹性体新的生物功能成为可能。
原文链接: