根据《柳叶刀》最新公布的报告“1990-2017年全球、区域和国家慢性肾脏病负担:2017年全球疾病负担研究的系统分析”指出,截至2017年,全球慢性肾脏病患者人数达6.975亿,其中中国肾病人数达1.323亿,患病率高达10%。中国在2014年的终末期肾脏病人(ESRD)患者接近200万人,按照美国肾脏病数据系统统计数据中慢性肾病最后发展为ESRD的比例1.5%进行推算,到2030年将达到315万人这一惊人的数字。ESRD患者需要终身进行透析以维持正常的生活需求,但是受各种因素的影响,中国ESRD患者接受血液透析治疗的比例仅为15%左右,远低于全球治疗率37%。随着医保覆盖率以及仪器普及率的提高,中国血透治疗的患者数量持续增长,成为极具潜力的蓝海市场,有望达到千亿规模。目前,国内高端血液透析器市场主要被德国费森尤斯、美国金宝、日本尼普洛等占据。高端血液透析器在医疗器械领域属于“卡脖子”的材料与技术,研发具有自主知识产权以及市场竞争力的血液透析器具有重要的民生和社会意义。
市场上主流的血液透析膜种类有聚砜膜PS(费森尤斯、贝朗、东丽、贝尔克、威高)、聚醚砜膜PES(欧赛、佩尼、尼普洛、贝尔克)、聚甲基丙烯酸甲酯PMMA(东丽)。但是,高分子材料血液相容性较差,在与血液接触时极易触发凝血瀑布导致血栓在透析膜表面形成,进而导致膜孔堵塞、膜通量大幅度衰减、毒素清除率降低;并且也会引发体内补体活化,使血液透析膜受到人体免疫系统的攻击。在临床应用中,通常需要注射肝素(未分级肝素或者低分子量肝素)以抑制透析器内血栓的形成。但是肝素的代谢困难,这对于一些出现出血症状的病人是不适用的,并且长期注射肝素还会导致血小板减少症、高钾血症、骨质疏松等。因此提高透析膜材料的血液相容性,研制自抗凝透析器,实现无肝素透析是目前血液透析的发展趋势。
中国科学院宁波材料技术与工程研究所刘富研究员团队自2014年就开始进行透析膜方面的系统研究,已经通过膜表面多巴胺固定肝素(Journal of Membrane Science 2014, 452, 390-399)、膜表面两性离子化(Journal of Membrane Science 2015, 475, 469-479)、表面亲水化(ACS Biomaterials Science & Engineering, 2016, 2 (12), 2207-2216)、膜表面水蛭素修饰(Journal of Membrane Science 2017, 523, 505-514)等方式改善材料的血液相容性,揭示了膜表面抗蛋白吸附和类肝素抗凝分子抑制凝血瀑布效应的机理,如图1所示。在此基础上,发展了系列抗凝涂层策略,在国内外率先实现了自抗凝透析器的制备,对于体外循环血液接触材料(如人工肾、人工肺ECMO及管路等)的血液相容性涂层的设计与制备具有重要意义。
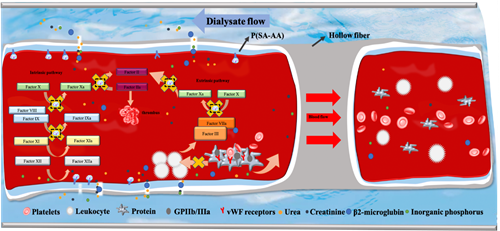
1)界面溶胀交联制备自抗凝透析器:中空纤维透析器由1万根中空纤维膜封装组成,膜丝的内径通常小于200 μm,在微米级的限域通道内实现亲水和抗凝分子的修饰具有非常大的挑战性。目前的许多研究工作通过物理共混或者化学接枝的方式实现材料抗凝性能的提高,但是改性物质与基体材料相容性的差异以及改性步骤的复杂性和不可控性,使得这些研究工作限制在平板膜上开展。针对该问题,研究团队发展了一种基于微孔膜的Top-down迁移及界面交联功能化策略(Journal of Membrane Science 2016, 520, 769-778,Journal of Membrane Science 2016, 513, 166-176),实现了抗凝分子在微孔膜表面的修饰,进一步地通过可控聚合技术合成了具有亲水基团(乙烯基吡咯烷酮)和抗凝基团(磺酸基团和羧酸基团)、具有序列排列结构的共聚物,通过微流控技术实现抗凝聚合物在透析器限域通道内的均匀分布,及界面交联固定,最终通过亲水基团的抗蛋白吸附以及磺酸羧酸基团的抗凝机理协同提高透析器的血液相容性。相关工作发表在Journal of Membrane Science 2018, 563, 115-125。
2)基于疏水相互作用制备自抗凝透析器:血液透析器中数量之多直径之细的中空纤维膜,使得残留的有机溶剂以及未反应的小分子单体很难清洗干净。因此,为了减少改性过程中的有机溶剂或化学分子残留,使用绿色环保溶剂以及减少改性过程中化学单体的使用量是极为有效的解决方式。常见的血液透析器多为高分子材质(如聚砜),其疏水特性很容易吸附血液中的蛋白质从而引发凝血瀑布产生血栓。研究团队通过自由基聚合的方式合成了一种两亲性聚合物聚(甲基丙烯酸月桂酯-对苯乙烯磺酸钠-丙烯酸)(P(LMA-SSNa-AA)),带有长烷基疏水侧链。两亲性聚合物可很好地分散于N,N-二甲基甲酰胺(DMF)/水(1:9,V)混合溶剂中,采用限域流控技术实现改性溶液在血液透析器内部循环,利用膜材料疏水吸附特性将类肝素改性物质均匀吸附在透析膜内表面。这种改性方式操作简单,改性体系组成简易,减少了有机溶剂参与,同时实现了透析器血液相容性的改善,对于后续的工业化生产和实际应用具有重要意义。相关工作发表于Journal of Membrane Science,2020, 595, 117593。
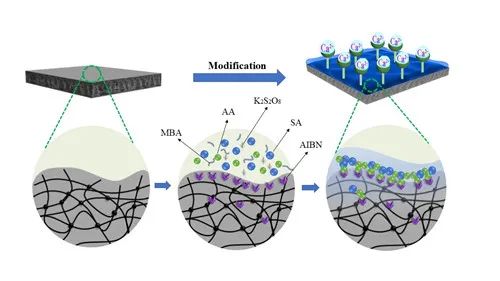
3)界面植入凝胶制备自抗凝透析器:为了实现改性过程无溶剂、绿色化,同时增强改性涂层与膜基体的结合力,防止改性涂层的脱落,研究团队将抗凝凝胶皮层通过界面植入的方式均匀地固定在中空纤维限域通道内,如图2所示。整个改性过程基于水体系,完全避免了透析器在清洗过程中的有机溶剂残留。基于对血液凝血级联反应的进一步理解,研究团队将海藻酸钠和丙烯酸合成了一种富含羧酸盐的改性聚合物,其抗凝机理不同于类肝素物质,对于膜材料表面的亲水性提高显著,并且能够螯合血液中的钙离子以阻断凝血瀑布。不仅能够提高透析膜的抗凝性能,对于抑制补体活性,防止免疫系统的激活同样具有十分优异的表现。偶氮二异丁腈(AIBN)为羧酸聚合物与基体材料的结合提供了连接点,通过控制AIBN的分布和植入量实现羧酸凝胶皮层的可控分布和厚度可控。该项工作已发表于Journal of Membrane Science, 2020, 604, 118082.。
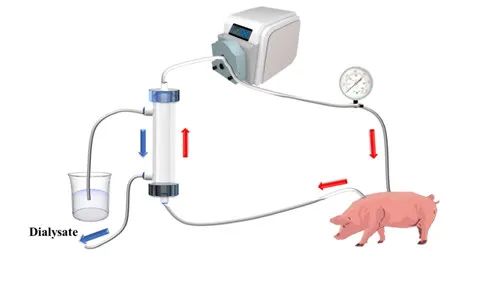
4)肾衰动物模型透析实验:在团队之前的工作中,已使用活化部分凝血酶时间(APTT)和凝血酶时间(TT)对改性透析器的抗凝时间做了相关测试。基于羧酸根和磺酸根的类肝素改性透析器的APTT>600s,基于羧酸根改性的透析器的APTT>360s;TT的时长相对于血浆也延长了数倍,证明改性之后的透析器均具有优异的抗凝特性。同时,使用酶联免疫吸附法表征了自抗凝透析器具有低的补体活性(C3a和C5a),基于实验室条件的限制,团队使用血浆和全血证明了改性透析器具有优异的血液相容性。为了进一步证明自抗凝透析器在临床具有实际应用价值,团队采用了由浙江中医药大学附属医院提供的肾脏衰竭的猪模型(尿素氮(BUN>6mmol/L)分别对上述的改性透析器进行时长为1h的少/无肝素透析实验,如图3所示,对透析过后的血液中的尿毒、肌酐、无机磷和β2-微球蛋白等小中分子毒素的含量进行测量,进行毒素清除率的计算。通过动物透析实验表征,三种改性透析器在减少肝素注射量或者不注射肝素的情况下都顺利完成了透析过程,与未改性透析器相比,改性透析器的外表面“挂血”现象得到了明显改善,并且中空纤维内表面残留的蛋白质和血栓数量也有显著减少,如图4所示。由于改性透析器亲水性的提高,三种改性透析器对于小中分子毒素的清除率得到了明显提高。关于三种改性透析器的性能对比和差异数据已经发表于《膜科学与技术》,2020, 40(1):84-92。

上述研究得到国家自然科学基金(51973230)、浙江省杰出青年科学基金(LR20E030002)、浙江省高层次人才青年拔尖(ZJWR0108020)、中国科学院青年创新促进会优秀会员(Y201848)、宁波科学技术局(2017C110034,2014B81004)的资助支持。


