通过左右晃动躲避攻击的蛇皮走位是DOTA等多人在线战术竞技游戏的一种进阶操作技巧。你可想过这种技巧除了游戏高手可以掌握外,由多个氨基酸缩聚而成的多肽(peptide)链也能表现?
美国弗吉尼亚理工化学系John B. Matson课题组和刘国良课题组合作,在JACS上报道了由四肽形成的多肽纳米带自组装为纳米螺旋的方法。通过向多肽纳米带体系中引入Ag+和聚磺苯乙烯钠 (PSSS)可使多肽纳米带“蛇皮走位”,形成纳米螺旋。此外,通过还原Ag+制备的多肽纳米螺旋-金属银复合物可作为表面增强拉曼散射(SERS)的基底。
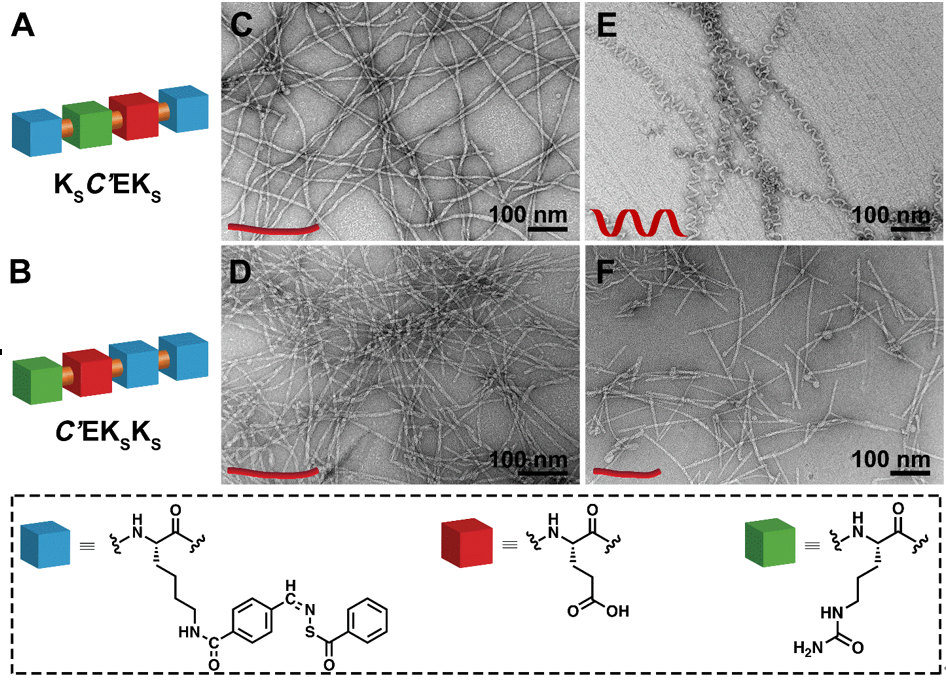
作者们首先合成了两种由同样氨基酸组成但排列顺序不同的四肽超分子聚合物同分异构体(KSC’EKS和C’EKSKS,图1A和B)。
透射电镜显示两种四肽在磷酸盐缓冲液中均呈纳米带形貌(图1C和D)。
然而当向缓冲液中加入AgNO3和PSSS后,KSC’EKS的形貌从纳米带演变成纳米螺旋(图1E),而C’EKSKS形貌无变化(图1F)。
多肽链的“蛇皮走位”与无机盐在水中解离出的正离子对KSC’EKS中谷氨酸羧基的屏蔽及KS在链中的位置有关。
AgNO3与PSSS的加入增加了KSC’EKS分子间的疏水作用,诱导其形成纳米螺旋,但未明显改变C’EKSKS分子间的作用力,因此后者形貌维持不变。
随后,作者们通过硼氢化钠还原银离子,发现有Ag纳米颗粒附着在多肽链上。该现象表明Ag+确有吸附在多肽链上。
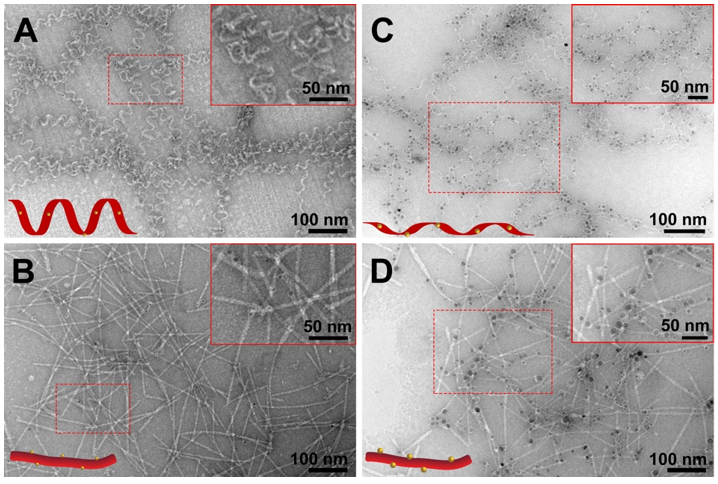
Ag纳米颗粒生长分两步:第一步形成平均直径2.8纳米、附着在多肽链上的银纳米种子(图2A和B)。
第二步继续向体系中引入Ag+和还原剂,利用前步生成的Ag颗粒作为生长核形成平均直径为7.6纳米的银纳米颗粒(图2C和D)。
透射电镜表明C’EKSKS纳米条带形貌在Ag生长前后保持不变,而KSC’EKS纳米螺旋的螺距变宽。
另外,Ag颗粒倾向沉积在KSC’EKS螺旋的凹陷处(图2C插图),而C’EKSKS纳米条带上Ag颗粒多附着在多肽的边缘,排列更无规(图2D插图)。
Ag纳米颗粒生长位置的不同对多肽-金属银复合物的物理性质有影响。
作者们探究了所合成的多肽-银复合物作为SERS基底的性能。
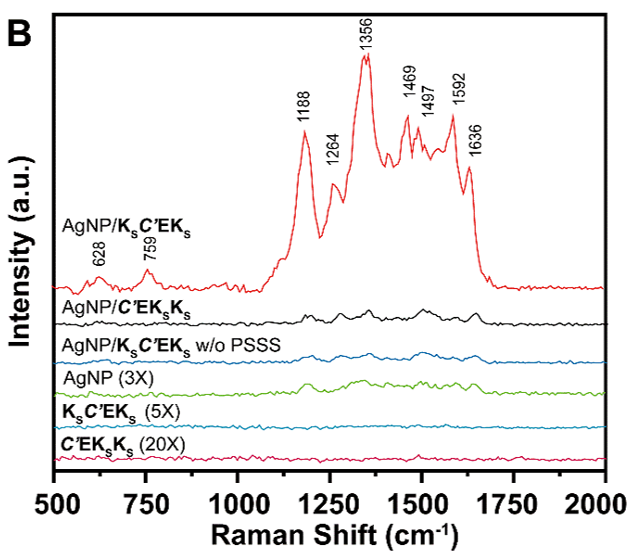
红色染料罗丹明B为被检测分子。实验结果显示(图3),附着有Ag颗粒的KSC’EKS纳米螺旋展现了显著的拉曼信号增强。
附着有Ag颗粒的C’EKSKS纳米带则与其他含银对照组SERS性能相当。不含Ag颗粒的两种多肽无明显信号增强性能。
该结果表明纳米螺旋结构是提升SERS性能的关键。采用2,2′-联吡啶为被探测物具有同样的SERS增强趋势。
作者们推测,Ag-纳米螺旋复合物的优异SERS性能得益于Ag颗粒的生长位置:位于螺旋凹陷处的Ag颗粒比位于多肽链表面的Ag颗粒更稳定,且螺旋有利于增大银颗粒空间分布密度,使得相邻银颗粒距离更近,增强效果好。相较于其他传统SERS基底,如纯金属颗粒或光刻蚀金属阵列,本工作报道的Ag-多肽基底具有独特的颗粒空间排列、易溶于水、更好的生物兼容性等优点。
原文:



