心脏肌肉组织支持着心脏在人一生中平均超过二十亿次的跳动。层状心肌纤维组成复杂的三维结构,为心肌组织提供同步收缩力。每一层心肌纤维都高度平行,以通过紧密的离子通道连接将电信号转成最大化的收缩力。如此复杂的微结构令到体外模拟心肌纤维与组织困难重重。更是令学习纤维结构的改变对心肌收缩力的影响和体外测药充满挑战。
近期加州大学圣地亚哥分校的Shaochen Chen教授实验室在《Biomaterials》杂志上发表了题为Direct 3D bioprinting of cardiac micro-tissues mimicking native myocardium的研究论文。作者们运用数字光处理3D生物打印技术和混合了高浓度心肌细胞的明胶衍生材料(GelMA),打印出设定的材料图案来诱导小鼠心室心肌细胞与纤维的排列(图1)。打印的心肌组织总长约2厘米,宽1厘米,厚250微米。心肌组织悬空在两个同时打印的微支柱(micro-cantilever)中间,以通过测量支柱位移来计算心肌收缩力(图1)。
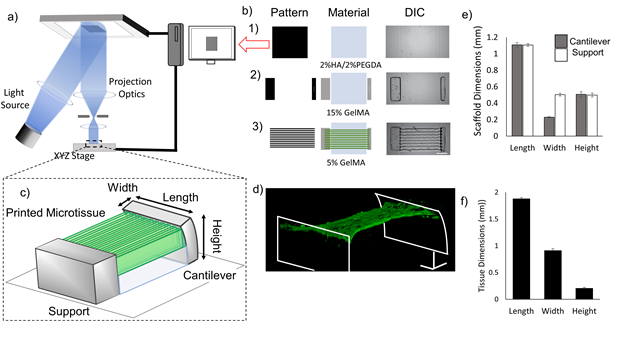
相较于在传统玻璃上的2D细胞培养和有平行图案诱导的2D培养,3D打印在微支柱间的样本展现出更一致的心肌纤维方向性。十天和三十天的样本表现出高度平行的肌原纤维节(sarcomere)以及更似体内心肌细胞的肌原纤维节长度(图2)。当肌原纤维节表现出一致的方向性与合适的长度,心肌组织产生的总体收缩力将提高并且趋近于体内心肌水平。

为了学习心肌纤维排列结构的改变对心肌收缩力和兴奋-收缩耦联 (excitation-contractioncoupling) 的影响,作者设计出不同的打印图案。通过改变明胶衍生材料(GelMa)的打印结构,小鼠心室心肌细胞与纤维的排列也相应改变(图3)。作者测试了五种打印图案,心肌纤维只有在平行图案打印出的材料中才显现出最大的收缩力和微支柱位移(图3)。
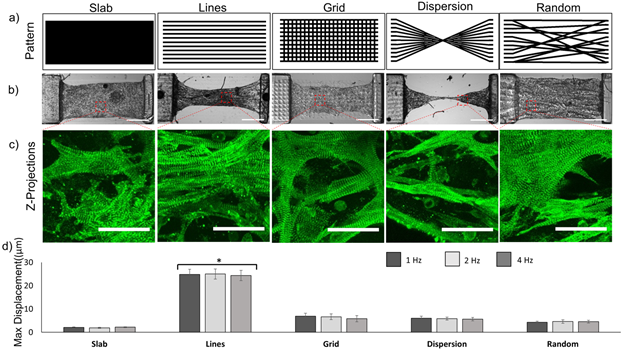
作者采用钙瞬变成像(calcium transient imaging)和异丙肾上腺素(isoproterenol)测试更进一步评估平行图案打印的心肌组织的兴奋-收缩耦联功能,也就是将离子电信号转变为收缩力的功能。作者发现未加异丙肾上腺素的样本已表现出与收缩力同时产生的瞬时性钙增高。通过比较异丙肾上腺素影响前后的样本,3D打印的心肌组织表现出预期的生理反应,也就是更快且更大的瞬时性钙增高现象(图4)。
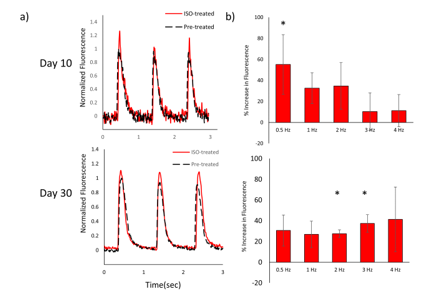
总结:通过数字光处理3D生物打印技术打印出的体外心肌组织结构有高通量,高重复性,可控性以及持久的生理成熟表现。通过打印图案的设计,心肌纤维可以高度平行排列并模拟体内微结构,同时产生最大化的收缩力。与心肌收缩力同时出现的瞬时性钙增高以及体外药物测试的生理反应更是说明3D打印心肌组织的成熟性。这样的心肌组织可以应用在更多的体外测药与心脏疾病研究。
参考文献:
Liu J, Miller K, Ma X, Dewan S, Lawrence N,Whang G, Chung P, McCulloch MD, Chen SC. Direct 3D bioprinting of cardiacmicro-tissues mimicking native myocardium. Biomaterials 2020. In Press.
文章链接:
https://www.sciencedirect.com/science/article/pii/S0142961220304506


