关节软骨是关节中的弹性结缔组织。软骨损伤是非常普遍的,但是由于其低细胞性和无血管性质,软骨具有有限的自我修复能力。由于软骨的损伤导致膝关节功能障碍,导致关节炎的关节严重疼痛和残疾,因此软骨或关节重建仍然是相当大的挑战。在临床实践中关节炎关节由全关节成形术使用金属和合成的假体。现有的关节假体不会与宿主关节组织重塑,并且可能因无菌性松动或感染而导致长期衰竭,只能通过关节的生物再生来解决。
使用间充质干细胞(MSC)移植,然后刺激定向分化为软骨细胞正在成为软骨修复的首选。近日,南京医科大学附属第一医院和上海交通大学医学院附属第九人民医院研究人员在《Science Advances》上发表了题为“3D bioprinting dual-factor releasing and gradient-structured constructs ready to implant for anisotropic cartilage regeneration”的研究论文,描述了三维(3D)生物打印双因子释放和梯度结构构造的各向异性软骨再生。
载有双因子的间充质干细胞(MSC)负载的水凝胶用于各向异性软骨形成的分化。3D生物打印各向异性软骨构造与赋予机械强度的物理梯度合成生物可降解聚合物一起,证明了整个层的完整性,表层的润滑以及深层的营养供应。在体外和体内对软骨组织的评估表明,组织的成熟和组织具有转化前景。
3D生物打印以制造双因子释放和梯度结构的软骨构建体
为了更好地模拟天然软骨,研究人员结合了具有不同生长因子释放的生化刺激(BCS)和具有较小孔径的生物力学刺激(BMS),以诱导更好的软骨形成,从而在创建了双因子释放和梯度结构的软骨构造刺激(DS)组。在软骨构造中,通过聚乳酸-乙醇酸共聚物(PLGA)(50:50 PLA / PGA)微球用于在水凝胶中递送TGFβ3和BMP4引入骨形态发生蛋白4(BMP4)和转化生长因子β3(TGFβ3)的组合。
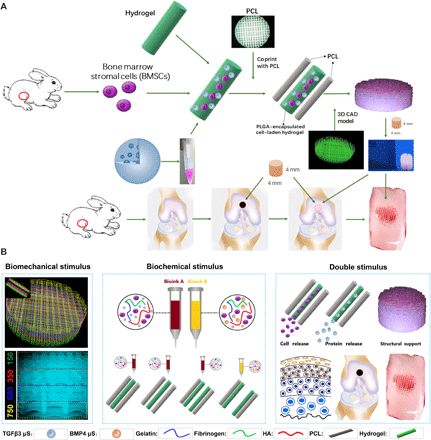
用于植入的3D生物打印梯度软骨支架
对于兔软骨构建体,支架为4×4×4 mm;对于人软骨构建体,则为14×14×14 mm。将TGFβ3和BMP4微球分别混合在充满细胞的水凝胶中,并使用不同的注射器将其印刷到PCL纤维之间的微通道中。为了化学模拟天然软骨中的肥大层,研究人员在最深的层中使用了PLGA BMP4包裹的MSC负载水凝胶,其PCL纤维间距为750μm,而PLGA-TGFβ3用于软骨构造的其他三层。
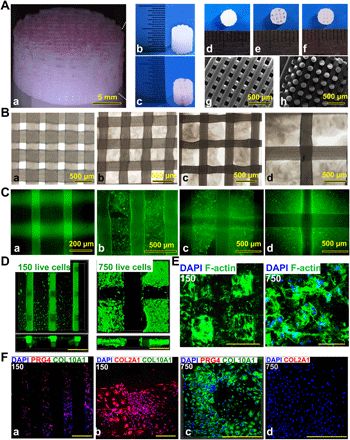
双重释放因子纳米颗粒对BMSCs体外存活和增殖的影响
在支架中检查了细胞活力和增殖。印刷的载有细胞的水凝胶使细胞沿印刷路径的纵向排列,形成具有细胞相互作用的网状网络。最终构建物中的PCL支柱结构进一步稳定了3D打印的BMSC组织,从而在充满细胞的水凝胶中诱导了细胞排列模式的压实现象。活/死细胞分析显示,第0天的细胞活力≥95%,在第3天到第21天保持超过75%的活力。表明一步法3D生物打印的双因子释放和梯度结构优化的软骨支架在打印过程中保留了细胞活力,并为BMSC的增殖,扩散和浓缩提供了有利的微环境,以在体外分化为软骨细胞。
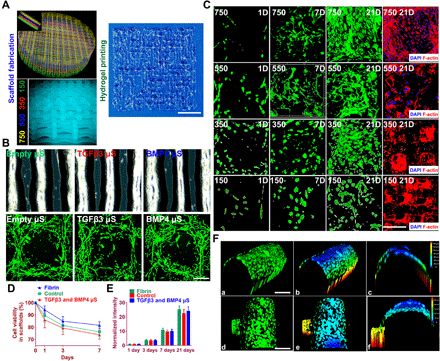
时空释放的rhTGFβ3和rhBMP4在3D生物打印的梯度结构支架中体外诱导软骨基质形成
在支架的体内应用之前,研究人员确定了rhTGFβ3和rhBMP4的时空传递是否诱导层特异性BMSC分化成软骨细胞并呈现出透明的关节和肥大的表型。
具有透明质和肥大表型的关节软骨细胞首先是从兔骨髓间充质干细胞体外获得的。透明质软骨细胞同时产生聚集蛋白聚糖和II型胶原,而肥大软骨细胞同时产生I型胶原和X型胶原。
在培养物中连续施用rhTGFβ3 2周,然后再进行rhTGFβ3 4周,诱导BMSCs分化为软骨细胞,该软骨细胞合成了聚集蛋白聚糖和II型胶原蛋白,表明是透明的关节软骨样细胞。。
此外,TGFβ3诱导的组织中的细胞是成纤维细胞,而BMP4诱导的细胞则更大,类似于先前在培养物中产生的肥大软骨细胞。两种处理均诱导BMSC分化并产生软骨基质,该基质在浓缩的BMSC中对甲苯胺蓝和阿尔辛蓝染色呈阳性,表明富含蛋白聚糖,软骨样ECM。
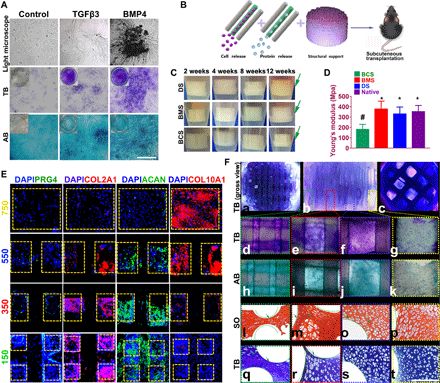
双因子释放和梯度结构支架在兔膝关节软骨缺损模型体内显示出更好的软骨修复效果
将兔用作动物模型以评估软骨支架的膝盖修复能力。与BCS和BMS支架相比,DS支架在第8、12和24周的软骨修复表现出更好的总体外观。在移植后的24周期间,对膝关节手术进行了磁共振成像,这表明DS组在24周后软骨下水肿的分辨率和关节表面的愈合明显更好。
此外,与NG组相比,梯度支架组在体内24周内显示出更好的软骨保护作用,组织学评分明显更高,在24周内具有更好的修复效果。DS各向异性支架比BCS或BMS组具有更好的软骨修复效果,并且移植后保持较好的关节功能。

双因子释放和梯度结构支架恢复了天然软骨的各向异性和更好的微血管向内生长
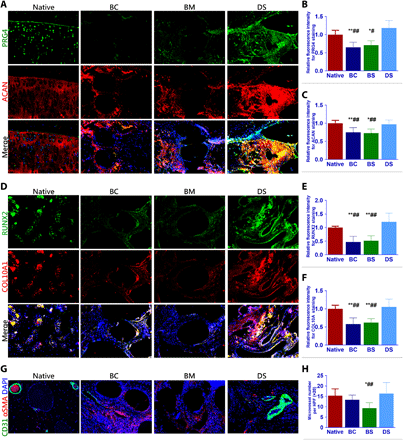
随着天然关节软骨从浅表层区域向深层区域的转变,不同表型的软骨细胞呈现出较高的润滑性和浅表层的GAG(PRG4,ACAN表达)以及深层的骨化(RUNX2,COL10A1表达)。
在本研究中,我们进一步测试了所生成软骨的各向异性,并将其与天然软骨进行了比较。在表层,免疫染色显示与其他两组相比,DS组和天然软骨中PRG4和ACAN的表达更高(图6,A至C)。
同时,植入双因子释放和梯度结构支架的组也观察到了骨化标记物(RUNX2和COL10A1)的较高表达(图6,D至F)。这些结果表明,双因子释放和梯度结构支架可以更好地恢复天然软骨在特定层中具有不同的成软骨和骨化标记物的各向异性。
此外,DS支架类似于天然软骨深层的向内生长的微血管,与孔径较小的组相比,DS支架可以更好地促进微血管向内生长,这表明在深部区域,孔径较大的组织具有更好的营养供应和组织整合。
展望
总之,研究人员设计了具有结构完整性的3D生物打印各向异性构造,用于关节重建和关节软骨再生,并进一步在兔软骨缺损模型中测试了功能性膝关节软骨构造。
通过顺序印刷带有梯度结构的合成PCL聚合物的蛋白释放蛋白和MSC载水凝胶,可以创建具有所需结构完整性并准备用于外科手术植入的人规模软骨构建体,该技术也可以用于再生软骨整个关节。与PCL支架相结合的打印为水凝胶提供了均匀性,并为体内研究提供了所需的机械性能。在本研究中,充满细胞的水凝胶可以使MSC和蛋白质包裹的微球分布均匀,从而保护细胞活力并促进其在支架中的分化和扩增。
同时,相邻的PCL脚手架提供了足够的机械支撑和结构完整性,为水凝胶中的3D锚定MSC细胞提供了稳定的微环境,以分化并形成组织,其分泌的软骨基质随着水凝胶的缓慢降解而替代了水凝胶。
全文链接:



