肿瘤血管的血栓闭塞可以阻断肿瘤的营养供给,诱导肿瘤细胞坏死,对癌症治疗特别有意义。但是这种促凝血形成血栓的疗法容易使肿瘤细胞产生耐药性,因此临床应用受限。同时,肿瘤复发是血栓疗法面临的另一个重要挑战,因为边缘的肿瘤细胞会向邻近的正常血管和组织汲取营养从而存活,造成复发。将肿瘤血管血栓闭塞和化疗药物结合能有效协同抑制肿瘤生长。但是促凝剂(造成血管栓塞)和化疗药物通常是分开给药的,并且需要仔细选择给药剂量和时间间隔,因为化疗药物的输送主要通过血管,而不理想的剂量和时间间隔可能导致两种疗法相互对立。
基于此,国家纳米科学中心的赵宇亮、吴雁和聂广军合作开发了一种同时负载凝血酶和化疗药物Dox的靶向肿瘤的离子凝胶纳米载体,避开了给药剂量和给药时间间隔的问题,从影响肿瘤血供和细胞增殖两个方面共同抑制小鼠及兔子乳腺癌肿瘤的生长。该工作发表在Nature Biomedical Engineering上。
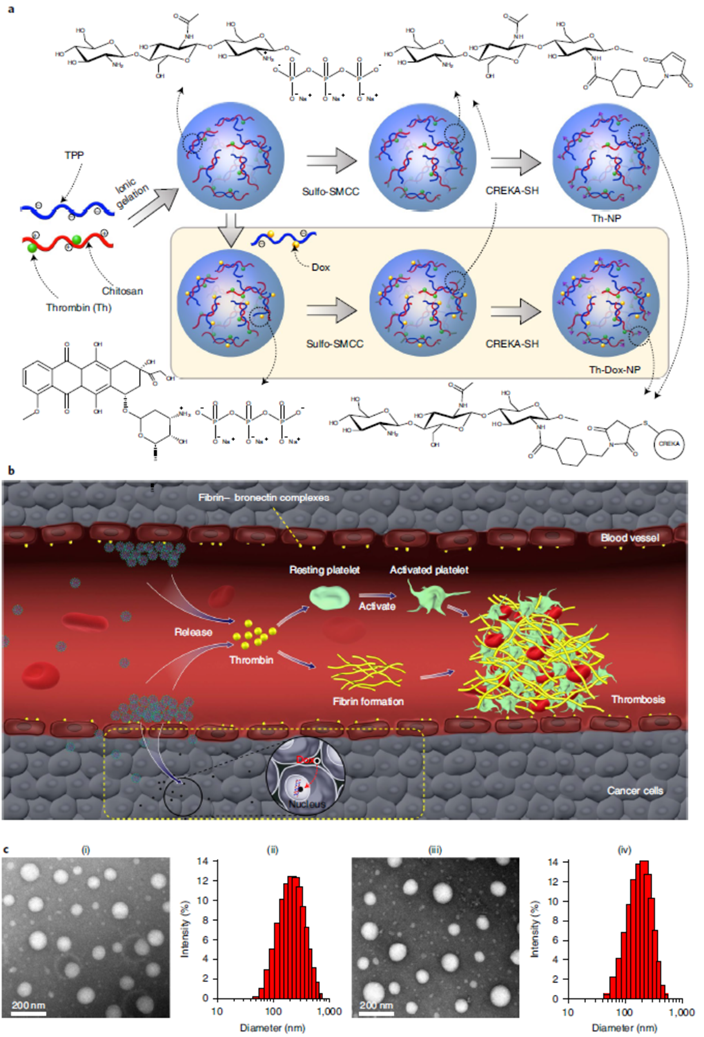
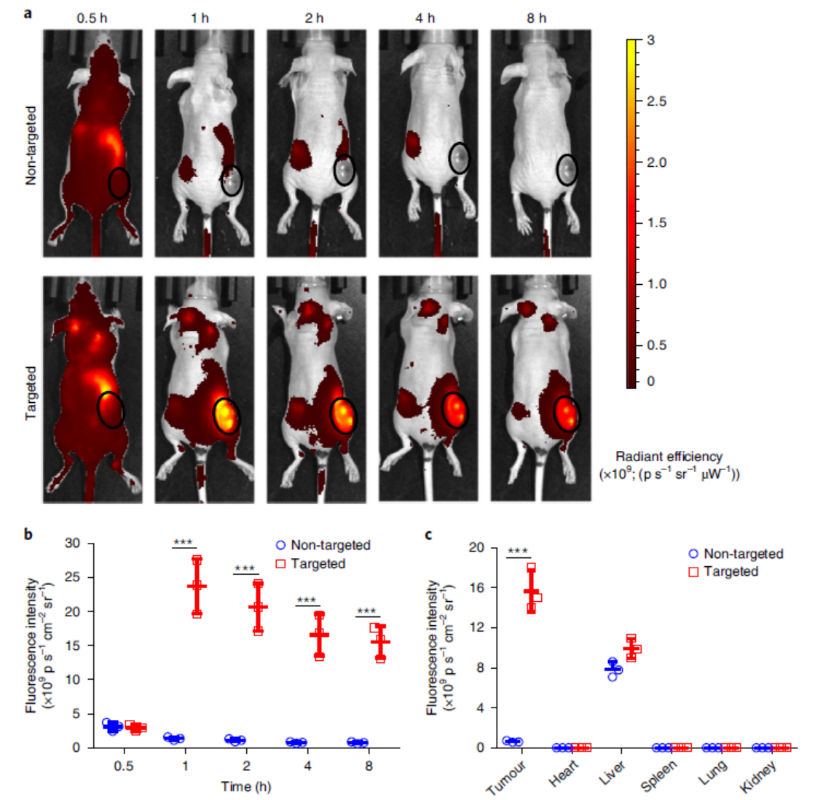
作者以生物可降解的壳聚糖为基础制备了负载凝血酶和Dox的、具有良好生物安全性的纳米凝胶,然后在纳米粒子表面修饰五肽CREKA,赋予纳米粒子肿瘤靶向能力。与非靶向对照组相比,8h尾静脉注射后,非靶组肿瘤部位基本没有纳米粒子,而具有靶向功能的纳米粒子更多地富集在肿瘤部位。优异的肿瘤靶向性可以增强纳米药物对肿瘤细胞的杀伤性,同时降低对正常细胞的伤害,减少副作用。
然后作者研究了肿瘤部位选择性血管栓塞的情况。经过纳米粒子治疗后的肿瘤有明显的淤伤和发黑的情况,正常部位不发生变化,且H&E染色发现,24h后在肿瘤血管中发现纤维蛋白血栓的存在,而生理盐水对照组则没用任何变化,证明纳米粒子成功将凝血酶靶向输送到肿瘤部位并引起血管破坏,造成肿瘤细胞坏死。
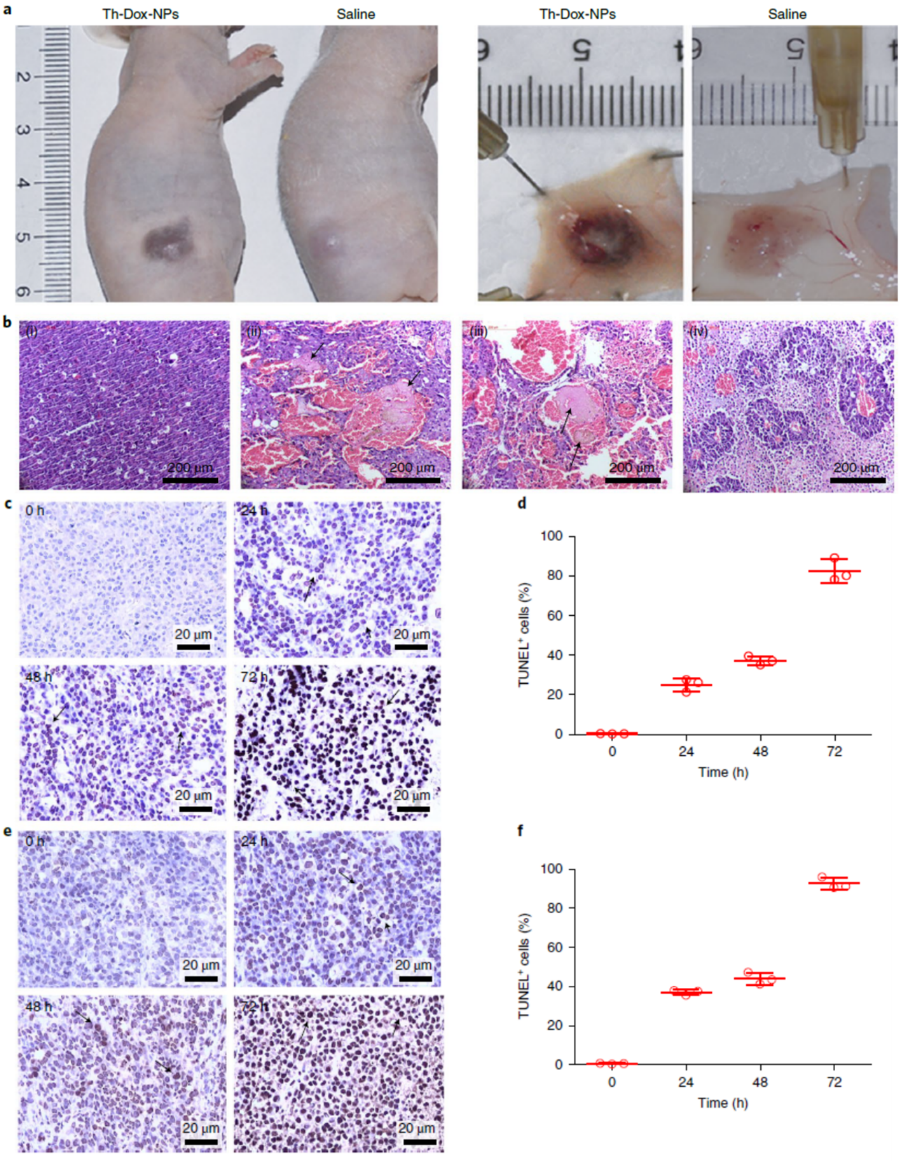
最后作者研究了肿瘤血管栓塞和化疗对肿瘤的协同治疗效果,发现这种共输送凝血酶和Dox的纳米粒子能明显减缓肿瘤增殖的趋势,延长小鼠的生存周期,并有效防止复发,比单一疗法有更好的治疗效果,在小鼠和兔子乳腺癌肿瘤均有良好的抑制作用。且作者使用壳聚糖材料,简单易得,生物安全性好,还绕开了凝血酶和化疗药给药剂量和时间间隔的问题,有望后期在临床中取得良好的效果。
原文链接:
https://www.nature.com/articles/s41551-020-0573-2


