近期,天津大学化工学院仰大勇教授课题组在化学领域权威期刊Angewandte Chemie(德国应用化学)上发表通过DNA动态组装在细胞内构建类细胞器结构并调控细胞行为的研究。天津大学化工学院郭小翠博士和李凤副教授为共同第一作者。相关成果已申请中国发明专利。研究得到国家自然科学基金等的资助支持。
细胞就像一个精密的小型工厂,细胞器是细胞内分工合作的车间,是细胞进行特定生化反应和执行特定生理功能的重要场所。通过在胞内原位构建类细胞器结构有望实现细胞功能重塑和疾病进程干预。
发展可精准调控的胞内原位动态组装系统,进而在复杂的胞内环境中实现分子精准可控动态组装和拓扑结构调控,是胞内原位构建类细胞器的重要途径,且存在极大的挑战和困难。迄今为止,胞内分子组装体系主要是基于酶响应的多肽类和合成高分子两类材料,在分子设计多样性、拓扑结构可控性和生物功能拓展性等方面仍存在局限。发展新型材料化学体系,开拓胞内动态组装新策略,是该领域实现突破的关键。脱氧核糖核酸(DNA)是一种符合精准材料化学理念的生物大分子,可实现分子的精准合成、精准操作、精准组装和对特定信号的精准响应,这些特点使得DNA在精准可控的动态组装材料中展现出独特优势(Chemical Reviews, 2020, https://doi.org/10.1021/acs.chemrev.0c00294)。
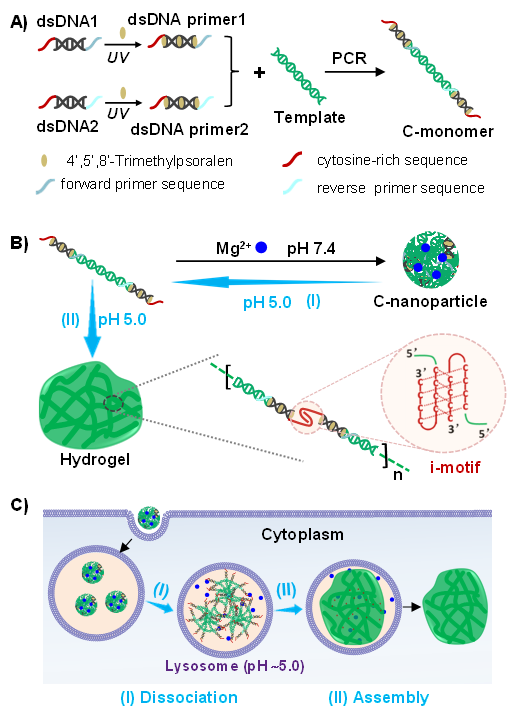
仰大勇教授课题组利用DNA的精准组装和刺激响应特性,构建了新型DNA动态组装系统,实现了DNA纳米颗粒在溶酶体酸性微环境中的拓扑变构,可在细胞内原位变构组装形成类细胞器DNA凝胶结构,并进一步研究了对细胞结构和行为的影响。作者利用化学交联的双链DNA作为引物,通过聚合酶链式反应制备了带有富含胞嘧啶(C)单链末端的双链DNA作为动态响应系统的结构基元(C-DNA)。
在酸性环境中,两个单链末端手拉手形成i-motif结构,从而C-DNA组装形成超长双链DNA,超长双链DNA进一步组装成纳米纤维,之后交织成三维网络凝胶结构。
作者将C-DNA压缩成DNA纳米颗粒;DNA纳米颗粒与细胞共孵育后通过溶酶体途径被细胞摄取;DNA纳米颗粒响应溶酶体的酸性微环境(pH5.0),发生原位拓扑变构形成凝胶结构,并逃逸至细胞质中,形成微米级的类细胞器结构。生物学效应研究表明,形成的类细胞器DNA凝胶结构可扰乱细胞骨架,使原本取向的细胞骨架变得扭曲无序,并使细胞触角变短。
细胞结构的改变进一步影响细胞的行为,促进细胞迁移。该工作不仅为细胞内原位构建类细胞器结构提供了新的材料体系和化学组装策略,同时为通过调控细胞内组装体的拓扑变构来调节细胞行为提供了启示,对理解细胞行为和纳米生物医学的发展具有重要的意义。
原文链接:


