尽管生物组织在本质上属于水凝胶材料,其中往往充满了体液,但在需要时,生物组织可以提高其自身的机械强度。例如,血液充血后肌肉变得更强。骨骼肌的收缩可以通过增加血流量来激活其相关的肌肉。因此,充血能导致肌肉硬度大大增加。这些系统溶胀增强性质的核心是组织中存在许多生物膜屏障,它们可以调节水分子和离子的跨膜运输。相比之下,人工合成的材料由于网络的稀释而呈现出典型的溶胀-弱化现象,溶胀后机械强度始终会急剧下降,并极大地限制了其应用,例如作为生物胶水或人工组织这类需要一定机械强度的场合。尽管研究表明,一些经过特殊设计的具有亲水-亲脂平衡的网络可以抵抗溶胀,但目前仍然难以制备能够增强溶胀后机械强度的聚合物材料。
上海交通大学医学院刘尽尧教授等人报道了通过生物启发策略实现的聚合物材料的溶胀强化现象。作者将脂质体膜纳米屏障共价嵌入交联网络中,以调节跨膜运输。溶胀后,拉伸的网络使脂质体变形,随后引发被包封分子的跨膜扩散,这可触发由预载前体形成新网络。由于双网状结构的坚韧性,该研究成功地实现了聚合物水凝胶的溶胀强化现象。膨胀触发的自增强功能可以用来开发各种动态材料。该研究以题为“Swelling-strengthening hydrogels by embedding with deformable nanobarriers”的论文发表在《Nature Communications》上。
【水凝胶的设计和准备】
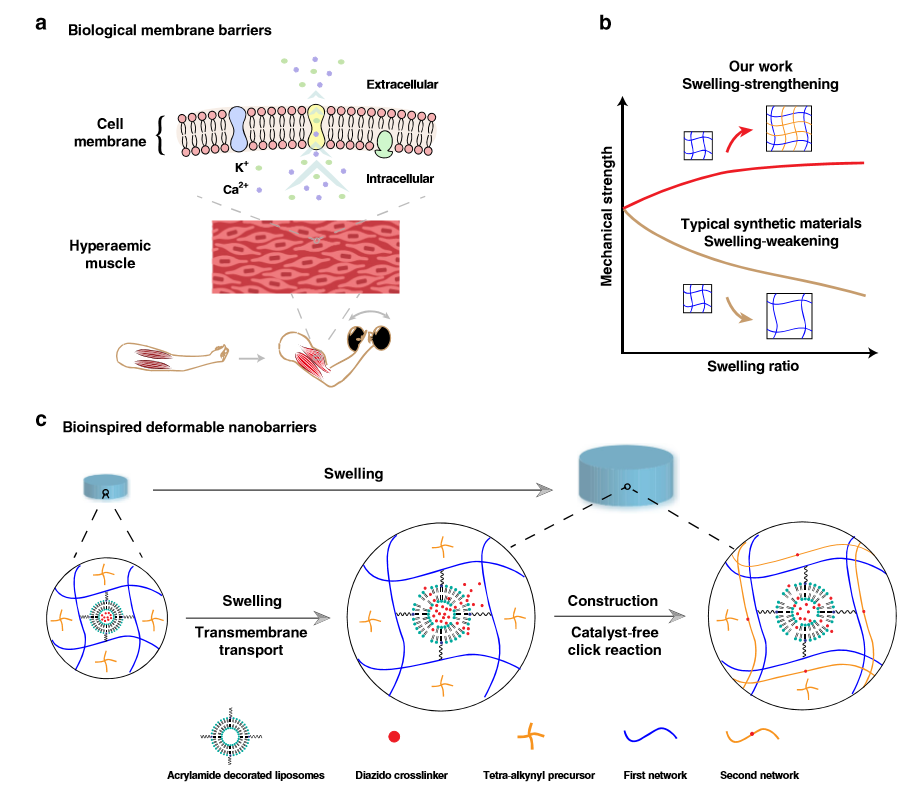
为了构建具有天然膜屏障功能的人工系统,作者设计将脂质体嵌入水凝胶材料中,以同时分离触发分子并调节其跨膜转运。该策略如图1c所示。装饰有双键的脂质体通过水基自由基聚合共价结合到第一个网络中。接下来将第二网络的前体预装在水凝胶中,并将可点击的交联剂分别预存储在脂质体内。交联剂的膨胀会触发跨膜传输,导致预加载的前体和分散的交联剂之间形成第二个聚合物网络。因此,当双网状结构形成导致强度增加超过溶胀引起的强度损失时,溶胀后的机械强度可能会超过初始强度。作为实验验证,作者通过将氢化大豆磷脂与胆固醇和二硬脂酰基磷酸乙醇胺-PEG2000-丙烯酰胺共同组装来制备具有双键修饰的脂质体。通过丙烯酰胺和N,N’-亚甲基双丙烯酰胺的水基自由基共聚,将装有N3-PEG3-N3的修饰脂质体共价连接至第一个网络。最后通过将Tetra-PEG-DBCO预装在聚丙烯酰胺(PAM)水凝胶中来获得溶胀强化的水凝胶(SSH)。
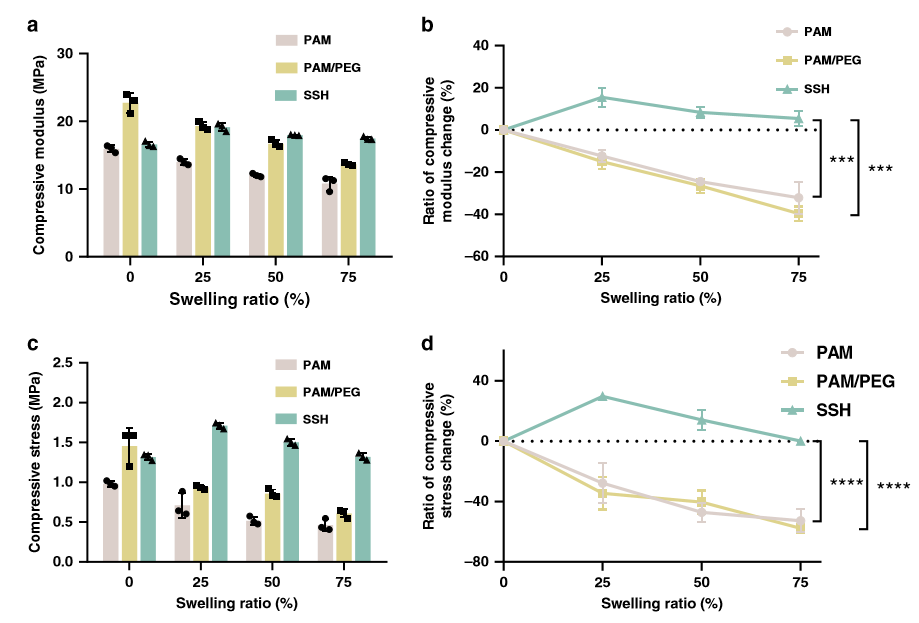
【溶胀强化行为】
如图2a,b所示,SSH的压缩模量以25%的溶胀率增加了15.6%±4.5。即使溶胀率增加到75%,SSH仍可以保留其初始机械强度。然而,对照水凝胶观察到典型的溶胀-弱化现象。相应的PAM单网络和PAM / PEG双网络水凝胶的溶胀模量在溶胀过程中持续下降,溶胀率为75%时分别下降32.1%±7.7和39.7%±3.4。
此外,随着溶胀率增加25%,SSH在90%应变下的压应力从1.32MPa增加到1.71MPa(图2c,d)。如预期的那样,两种对照水凝胶在90%应变下的压缩应力大大降低,并且在75%的溶胀率下分别降低了52.8%±7.7和57.7%±3.2。这可以通过SSH中大量交联脂质体的存在来解释,这增加了凝胶的机械强度。然后作者将SSHs皮下植入大鼠背部,以研究其在生理环境中的溶胀强化行为(图3a,b),结果表明SSH在复杂的体内条件下同样表现出出色的溶胀强化行为。
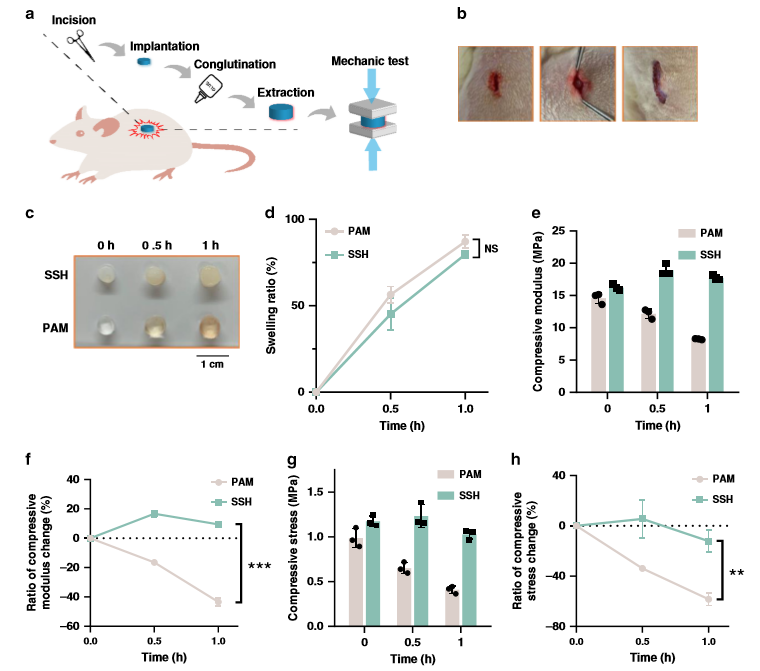
【双网络的形成】
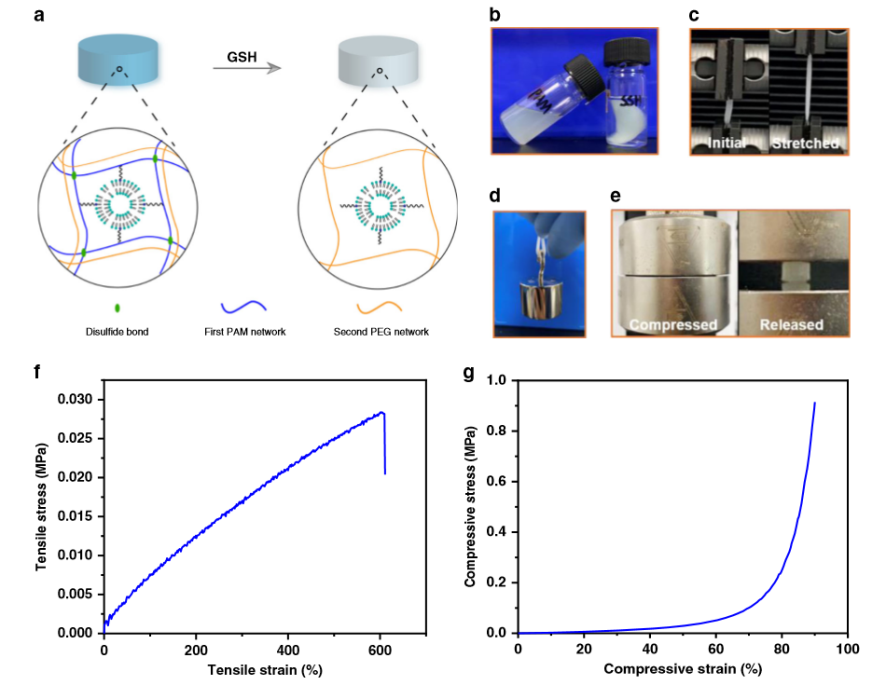
为了进一步确定第二个网络的结构,作者设计并合成了可触发的PAM网络,该网络可以全面表征新形成的网络(图4a)。因此,在形成双网状结构后,初始网络可被还原剂谷胱甘肽(GSH)溶解。删除第一个网络后,即可获得新形成的网络。
如图5b所示,二硫化交联的PAM网络被GSH触发溶解。正如预期的那样,溶胀的水凝胶经过GSH处理后可以保持其初始固体形状(图5b-e),从而验证了第二个网络的形成。通过扩散完全除去交联的PAM,可以得到单一的第二网络。机械测试表明,形成的第二网络在600%应变下的拉应力为28.4kPa,在90%应变下的压应力为915kPa(图5f,g)。这些结果很好地证实了SSH的机械性能、微观形态和分子结构。
总结:作者报道了一种借助生物膜屏障启发策略实现的溶胀强化水凝胶(SSH),将共价嵌入交联网络中的脂质体膜纳米屏障用于调节跨膜运输。
溶胀后,拉伸的网络使嵌入的膜纳米屏障变形,随后引发被包封分子的跨膜扩散,这可触发由预载前体形成新网络并形成双网络结构。
由于双网络水凝胶的坚韧特性,SSH无需外部刺激和其他添加剂的帮助即可显示出其膨胀强化行为。膨胀触发的自增强功能可以制备各种动态材料,这可能会大大扩展其在生理环境中的应用。
原文链接:



